Часть 2 / Часть 1
Антиконвульсанты
Карбамазепин
Greil et al. (1997, 1999) в открытом контролируемом испытании сравнивали карбамазепин и литий у 144 пациентов с БАР I и II на протяжении 2,5 лет.
Не отмечалось различий между обоими видами лечения при анализе выживаемости до следующей госпитализации или возврата симптомов аффективного эпизода, однако при учете других клинически важных показателей литий значимо превосходил карбамазепин.
Дисклеймер
Эта статья предназначена исключительно для информационных и образовательных целей.
Она не является медицинским советом или рекомендацией и не должна рассматриваться как замена консультации с квалифицированным специалистом в области психического здоровья.
Если вы или кто-то из ваших близких испытываете симптомы психического расстройства, пожалуйста, обратитесь за помощью к психиатру.
Симптомы могут быть индивидуальны и варьироваться у разных людей, и только профессионал может определить точный диагноз и назначить соответствующее лечение.
В других испытаниях не удалось показать преимущество карбамазепина перед плацебо при профилактической терапии (Bandelow et al., 2008). (Уровень доказательности F для профилактики маниакальных и новых депрессивных эпизодов, уровень доказательности С для профилактики любых аффективных эпизодов.)
В исследовании Denicoff et al. (1997) литий и карбамазепин по отдельности сравнивали с комбинацией обоих препаратов у пациентов с быстрой цикличностью. И то, и другое средство показало плохой терапевтический ответ.
В одном открытом испытании и в серии случаев сообщалось о некотором положительном эффекте карбамазепина у лиц с быстрой цикличностью, однако контролируемые доказательства отсутствуют (Joyce, 1988; Riemann et al., 1993). (Уровень доказательности F у пациентов с быстрой цикличностью.)
Рассматривая результаты различных исследований в специфических подгруппах пациентов, карбамазепин можно считать эффективным в случае неполного терапевтического ответа на лечение литием или быстрой цикличности, при сопутствующих органических (неврологических), а также шизоаффективных расстройствах (Denicoff et al., 1997; Schneck, 2002; Elphick, 1985; Goncalves, Stoll, 1985; Greil et al., 1997) (оценка «++» для дополнительных доказательств).
Проблемы с переносимостью карбамазепина возникают редко. Наиболее частые побочные эффекты включают атаксию, тошноту, головокружение, нечеткость зрения и диплопию.
Реже встречаются выпадение волос, светочувствительность, полиурия, эректильная дисфункция, головные боли, шум в ушах, сухость во рту и запоры. Потенциально угрожающие жизни побочные явления включают аллергические реакции (синдром Стивенса – Джонсона), гипонатриемию, печеночную недостаточность, агранулоцитоз и другие нарушения со стороны крови с риском кровотечений.
Карбамазепин является тератогенным препаратом, риск дефектов невральной трубки составляет 0,5-1%, поэтому следует избегать его назначения во время беременности (Ernst, Goldberg, 2002). (Оценка «–» для безопасности и переносимости.)
Существуют только спорадические сообщения о влиянии карбамазепина на суицидальные намерения. Данные нескольких исследований указывают, что в профилактике суицидов и суицидальных намерений карбамазепин уступает литию.
Также отсутствуют доказательства того, что карбамазепин повышает риск суицидов (Thies-Flechtner et al., 1996; Greil et al., 1997; Born et al., 2005). (Оценка 0 для профилактики суицидов.)
Карбамазепин в большинстве стран доступен в виде таблеток или раствора для перорального приема. Рекомендуемый уровень концентрации в плазме крови для профилактики возврата симптомов составляет 4-12 мг/л, хотя эти данные экстраполированы из исследований у лиц с эпилепсией.
При использовании с профилактической целью у эутимических пациентов дозу препарата следует повышать постепенно медленно, также могут применяться стратегии быстрого наращивания дозы (Weisler et al., 2006). При комбинированном лечении серьезным недостатком является индукция различных ферментов цитохрома P450 (Spina et al., 1996).
Это может вызывать усиление метаболизма АД и АП, в частности оланзапина, кветиапина и рисперидона, что приводит к уменьшению их эффективности (Tohen et al., 2008; Fitzgerald, Okos, 2002; Yatham et al., 2003). Кроме того, карбамазепин взаимодействует с вальпроатом и ламотриджином, а также с контрацептивами. (Оценка «–» для практичности.)
Доказательства длительного приема карбамазепина получены из исследований с низкой силой эффекта или открытых испытаний, что снижает степень рекомендаций. Кроме того, ограниченны данные о проблемах с переносимостью препарата. Помимо прочего, карбамазепин обладает высоким потенциалом лекарственных взаимодействий. (Степень рекомендаций 3.)
Ламотриджин
В двух двойных слепых РКИ были представлены доказательства эффективности ламотриджина для профилактики эпизодов, вызванных лечением (Bowden et al., 2003; Calabrese et al., 2003).
В обоих исследованиях показано значимое увеличение времени до необходимости лечения следующего эпизода при приеме лития и ламотриджина по сравнению с плацебо. При совокупном анализе обоих испытаний ламотриджин превосходил плацебо по времени возникновения новых любых, маниакальных и депрессивных эпизодов (p = 0,033) (Goodwin et al., 2004).
Была предпринята попытка при вторичном анализе результатов выявить различия между временем возврата симптомов и рецидивов. Оказалось, что при приеме обоих препаратов среди пациентов, у которых перед назначением профилактического лечения была достигнута стабилизация состояния, время до следующего аффективного эпизода было значимо большим (Calabrese et al., 2006).
В клинической практике ламотриджин часто назначается пациентам, у которых преобладает депрессивная полярность БАР (Grande et al., 2012). (Уровень доказательности D для профилактики маниакальных эпизодов, уровень доказательности A для профилактики любых аффективных и депрессивных эпизодов.)
Кроме того, проведено два исследования, в центре внимания которых была оценка эффективности ламотриджина у пациентов с быстрой цикличностью.
В одном из них (SCAA, 2012) ламотриджин двойным слепым образом использовался в качестве дополнения к лечению другими психотропными средствами, но не литием или вальпроатом. Через 6 месяцев ламотриджин не был эффективнее плацебо у пациентов с БАР II, но не с БАР I (Denicoff et al., 2002; Goldberg et al., 2008).
В другом испытании ламотриджин также не превосходил плацебо у больных с быстрой цикличностью. (Уровень доказательности E у пациентов с быстрой цикличностью.)
В РКИ van der Loos et al. (2009) были получены дополнительные доказательства эффективности использования комбинации ламотриджина с литием у лиц с недостаточным терапевтическим ответом на монотерапию последним. В РКИ Licht et al. (2010) сравнивали эффективность ламотриджина (n = 77) и лития (n = 78) у эутимических пациентов, период катамнестического наблюдения составил более 5 лет.
Статистически значимые отличия между обоими препаратами отсутствовали. В датском исследовании Kessing et al. (2011) отметили, что литий может быть несколько эффективнее ламотриджина, особенно при более длительной продолжительности катамнестического наблюдения.
Кроме того, эффективность применения ламотриджина в профилактическом лечении подтверждена в трех метаанализах (Smith et al., 2007; Beynon et al., 2009; Vieta et al., 2011). (Оценка «+» для дополнительных доказательств.)
Ламотриджин обычно хорошо переносится и является препаратом выбора для профилактического лечения. Совокупный анализ двух РКИ, проведенный Goodwin et al. (2004), показал, что в открытых исследованиях у 11% пациентов отмечались кожные высыпания, а в двойной слепой фазе частота последних, а также таких побочных эффектов, как головная боль, тошнота и диарея не отличалась от таковой в группах плацебо.
Тяжелые кожные высыпания и аллергические реакции случаются редко (приблизительно до 0,08% при монотерапии и до 0,13% при комбинированном лечении среди взрослых в двойных слепых РКИ).
Как правило, при их возникновении рекомендуется постепенное повышение дозы препарата (Seo et al., 2011). Преимуществом при длительном лечении ламотриджином считается его благоприятный метаболический профиль. FDA рекомендует не назначать препарат в дозе выше 200 мг/сут во время беременности (Morrow et al., 2006). (Оценка «+» для безопасности и переносимости.)
В 2008 г. в докладе FDA, где были проанализированы результаты 199 РКИ использования 11 противоэпилептических средств, указывалось, что ламотриджин может вызывать суицидальные намерения (95% доверительный интервал [ДИ] 1,03-4,40). Однако результаты лечения исключительно пациентов с БАР противоречат этому выводу (Fountoulakis et al., 2012; Gibbons et al., 2009). (Оценка 0 для профилактики суицидов.)
В большинстве стран ламотриджин доступен в виде таблеток (от 2 до 200 мг), а также растворимых в воде таблеток. Рекомендуемый безопасный уровень концентрации в плазме крови при эпилепсии составляет 3-14 мг/л (11,7-56,4 мкмоль/л) (Neels et al., 2004).
Так, существует прямая пропорциональная зависимость между дозой препарата и концентрацией в плазме. У пациентов с БАР целесообразно постепенно наращивать дозу ламотриджина до 200 мг/сут на протяжении 6 недель. Ламотриджин обладает значительными лекарственными взаимодействиями с карбамазепином, вальпроатом и этинилэстрадиолом (содержится в оральных контрацептивах).
При одновременном назначении с карбамазепином дозу ламотриджина следует увеличивать в два раза, с оральными контрацептивами – наполовину и снижать при приеме с вальпроатом (Johannessen, Landmark, 2010). (Оценка 0 для практичности использования.)
Установлена степень рекомендаций 1 для применения ламотриджина у пациентов, которые хорошо переносят препарат, когда основной целью является профилактика возврата симптомов депрессивных или любых аффективных эпизодов. С учетом указанных выше замечаний, не исключается использование препарата в определенных клинических ситуациях у больных других групп.
Литий
Большинство РКИ эффективности лития, в которых отмечалось снижение частоты аффективных эпизодов БАР, проведены в 70-е гг. прошлого века. Недавние обзоры этих исследований продемонстрировали, что во многих из них клиническая польза лития могла быть переоценена, кроме того, они не соответствуют современным методологическим требованиям, хотя это не уменьшает их значение (Goodwin, Jamison, 2007; Maj, 2000; Licht, 2012).
До сегодняшнего дня сохраняют свое значение выявленные в них предикторы хорошего терапевтического ответа при лечении литием, такие как семейный анамнез БАР, интервалы без маниакальных или депрессивных эпизодов, отсутствие быстрой цикличности, злоупотребления алкоголем или наркотиками и, в особенности, хорошее соблюдение приема препарата (Grof, 1979).
Начиная с 90-х гг., проводились испытания, в которых литий сравнивался с другими психотропными средствами.
Литий превосходил плацебо во времени до необходимости начала лечения возврата симптомов маниакального и/или депрессивного эпизода в исследовании эффективности кветиапина, а также маниакального эпизода в двух испытаниях при изучении ламотриджина, что подтверждалось при совокупном анализе этих наблюдений (Weisler et al., 2011; Bowden et al., 2003; Calabrese et al., 2003; Goodwin et al., 2004). (Уровень доказательности A для профилактики любых аффективных и маниакальных эпизодов и уровень доказательности D для профилактики депрессивных эпизодов.)
Долгое время на основании имевшихся наблюдений профилактическое действие лития у пациентов с быстрой цикличностью оценивалось низко (Dunner, Fieve, 1974; Dunner, 1998). Однако результаты непосредственного сравнения лития с вальпроатом в двойном слепом РКИ свидетельствуют о том, что между этими двумя препаратами отсутствуют статистически значимые различия (Calabrese et al., 2005).
Однако по причине высокого уровня прекращения испытаний (до 76%) выводы этого исследования не являются окончательными. В другом двойном слепом испытании литий сравнивался с комбинацией лития и вальпроата у биполярных пациентов с быстрой цикличностью и сопутствующим злоупотреблением психоактивными веществами (Kemp et al., 2009).
В ходе наблюдения также был высоким уровень прекращения приема препаратов (до 79%), поскольку у многих больных не достигалась стабилизация состояния. (Уровень доказательности F при быстрой цикличности.)
В нескольких исследованиях была подтверждена эффективность применения лития для профилактики любых аффективных рецидивов и маниакальных рецидивов (Geddes et al., 2004; Smith et al., 2007; Beynon et al., 2009; Vieta et al., 2011).
Однако доказательств, поддерживающих эффективность лития в профилактике биполярной депрессии, недостаточно (Weisler et al., 2011).
При непосредственном сравнении лития с оланзапином в условиях двойного слепого РКИ у стабилизированных пациентов на протяжении одного года литий не превосходил оланзапин для профилактики эпизодов, вызванных лечением.
Также оланзапин значимо снижал риск возврата/рецидива маниакальных эпизодов, и не наблюдалось различий между препаратами в профилактике возврата депрессии (Tohen et al., 2005). Кроме того, следует отметить, что это испытание финансировалось производителем оланзапина.
Также было выполнено два исследования, посвященных сравнению ламотриджина с литием. Так, Kessing et al. (2011) сравнивали необходимость перехода к другому лечению, дополнения терапии или психиатрической госпитализации при применении ламотриджина или лития.
Для ламотриджина была выявлена более высокая вероятность изменения или дополнения лечения, чем для лития (относительный риск [ОР] 2,60; 95% ДИ 2,23-3,04), независимо от типа эпизода (депрессивный, маниакальный, смешанный) или ремиссии.
Кроме того, при приеме ламотриджина возрастала вероятность госпитализации (ОР 1,45; 95% ДИ 1,28-1,65), а также повышался уровень необходимости лечения депрессивных (ОР 1,31; 95% ДИ 1,01-1,70) и маниакальных (ОР 1,65; 95% ДИ 1,31-2,09) эпизодов. Для смешанных эпизодов и у пациентов в состоянии ремиссии данный уровень не различался.
Однако в проведенном исследовании могла присутствовать предвзятость при отборе пациентов, что следует учитывать при интерпретации полученных данных.
Национальным институтом психического здоровья США было проведено сравнительное исследование эффективности лития и оптимизированного лечения без данного препарата у пациентов с клинически значимыми симптомами БАР (Nierenberg et al., 2009).
Несмотря на использование большого количества методик оценки результата, ни по одной из них в двух группах пациентов не наблюдалось отличий к 6-му месяцу катамнестического наблюдения. Однако это испытание было недостаточно продолжительным, чтобы установить все аспекты профилактического применения лития.
В определенной степени представляется, что литий способствует достижению и поддержанию полной (а также функциональной) ремиссии у значительной части биполярных больных. Grof предложил использовать термин «отличный терапевтический ответ на лечение литием» для пациентов, жизнь которых кардинально изменилась благодаря профилактической терапии.
Было выявлено, что наилучший терапевтический ответ отмечался у больных, расстройство у которых характеризовалось эпизодическим клиническим течением, полными ремиссиями, семейным анамнезом БАР и малой отягощенностью сопутствующими психиатрическими заболеваниями (Grof, 2010).
Полное функциональное выздоровление при лечении литием также могло способствовать сохранению когнитивного функционирования на таком же уровне, как и у здоровых контрольных субъектов (Rybakowski, Suwalska, 2010). (Оценка «++» для дополнительных доказательств.)
Литий обладает низким терапевтическим индексом. Таким образом, превышение терапевтической концентрации препарата в крови иногда может привести к серьезным токсическим и потенциально летальным последствиям для ЦНС. Подобное также может относиться к дегидратации. Как известно, побочные эффекты лития в большинстве случаев зависят от уровня концентрации препарата в плазме.
До 75% пациентов, принимающих литий, испытывают легкие нежелательные явления (преходящий металлический привкус во рту, полиурия, полидипсия, повышение веса, отечность, трудности концентрации и сонливость), которые могут быть устранены путем уменьшения дозы или отмены препарата.
При высокой концентрации лития в крови до 65% больных отмечают побочные реакции со стороны ЦНС, в частности тремор, который, вероятно, является проявлением токсичности. Также признаками токсичности могут быть тошнота, диарея и нечеткость зрения (Freeman, 2006).
Эти эффекты иногда усиливаются, а риск токсичности может возрастать при комбинации лития с другими средствами, например типичными АП или карбамазепином, а также у лиц с неврологическими заболеваниями в анамнезе (Sachdev, 1986; Shukla et al., 1984; Moskowitz, Altshuler, 1991).
С точки зрения пациентов, наибольшее беспокойство у них вызывают, кроме указанных побочных эффектов, ухудшение когнитивных функций и/или снижение интенсивности восприятия и эмоций (Licht, 2012).
Длительный прием лития может влиять на функции почек (Tredget et al., 2010; Bendz et al., 2010). Часто, особенно у женщин, имеет место гипотиреоидизм, требующий назначения заместительной терапии (Johnston, Eagles 1999).
Литий обладает тератогенными эффектами (Yonkers et al., 2004; Nguyen et al., 2009). Во время беременности оправданной считается отмена препарата (Baldessarini et al., 1999). При длительном приеме лития описаны редкие случаи гипопаратиреоидизма с нарушениями обмена кальция (McKnight et al., 2012). (Оценка «–» для безопасности и переносимости.)
Существует значительное количество доказательств специфического антисуицидального действия лития, которое не зависит от улучшений при аффективном расстройстве. Литий обладает антиагрессивными и антиимпульсивными свойствами, с которыми также может быть связан антисуицидальный эффект (Kovacsics et al., 2009; Cipriani et al., 2005).
У пациентов, принимавших литий, с меньшей вероятностью отмечался летальный исход в результате суицида (отношение шансов [ОШ] 0,26; 95% ДИ 0,09-0,77). Также у них имел место более низкий риск нанесения самоповреждений (ОШ 0,21; 95% ДИ 0,08-0,50).
Схожие данные были получены в крупном обсервационном исследовании, проведенном в Швейцарии (Angst et al., 2002). Более подробно этот вопрос освещен в работах Baldessarini et al. (2006), Gonzalez-Pinto et al. (2006), Muller-Oerlinghausen et al. (2006) и Wasserman et al. (2012). (Оценка «++» для профилактики суицидов.)
Для лечения БАР доступны различные соли лития: лития карбонат, лития цитрат, лития гидрогенаспартат. Также имеются таблетки с длительным высвобождением и сироп в каплях (только лития цитрат). Отсутствуют доказательства различий между солями лития, формы препарата обладают незначительными отличиями в переносимости.
В большинстве случаев дозу лития медленно повышают в зависимости от индивидуального опыта и данных мониторинга концентрации в плазме крови (Abou-Auda et al., 2008).
Учитывая очень узкие безопасные границы, уровень концентрации лития в сыворотке крови следует часто и регулярно проверять до/после достижения терапевтического уровня. Рекомендуется выполнять проверку каждые 3-6 месяцев у пациентов со стабильным уровнем концентрации и всегда при изменениях клинического состояния, соматических заболеваниях или одновременном назначении с другими медикаментами (например, фуросемидом) (Zarin et al., 2002).
Кроме того, необходимо регулярно следить за функциями почек и щитовидной железы каждые 6-12 месяцев в зависимости от риска.
Уровень концентрации лития в плазме крови для успешной профилактики мании, вероятно, отличается от такового для профилактики депрессии. Так, в РКИ Severus et al. (2010) содержание лития 0,6 ммоль/л представлялось неэффективным для профилактики маний, но достаточным для профилактики депрессии.
Более высокие концентрации не обязательно предотвращают повторное появление симптомов депрессии, однако способствуют профилактике новых маниакальных эпизодов (Kleindienst et al., 2007; Severus et al., 2009).
В метаанализе Severus et al. (2010) сделан вывод, что минимальная эффективная концентрация лития в плазме крови при БАР составляла 0,4 ммоль/л, а оптимальный терапевтический ответ достигался при 0,6-0,75 ммоль/л. Содержание 0,75 ммоль/л не оказывает влияние на все проявления заболевания, однако может улучшать контроль над симптомами между маниакальными эпизодами.
Помимо этого, резкое снижение концентрации более чем на 0,2 ммоль/л связано с риском рецидива (Severus et al., 2010). Несмотря на указанные рекомендации, следует помнить, что индивидуальные оптимальные концентрации могут варьировать.
Часто возникает вопрос о необходимости отмены лития. Так, установлен высокий риск рецидива после прекращения его применения, а возобновление приема не всегда может быть эффективным (Mander, Loudon, 1988; Post et al., 1992; Goodwin, 1994). В случае необходимости поддерживающую терапию литием настоятельно рекомендуется сокращать постепенно на протяжении нескольких недель или даже месяцев (Suppes et al., 1993).
Перед началом терапии пациента всегда следует подробно инструктировать о проявлениях токсичности и ситуациях риска (Licht, 2012). (Оценка «–» для практичности.)
При сравнении с другими средствами, которые применяются для профилактического лечения, литий обладает наиболее высокими оценками доказательств для любых рецидивов и мании, а также уровнем доказательности B для депрессии.
Кроме того, литий оказывает антисуицидальный эффект. По сравнению с другими препаратами литий вызывает больше проблем с применением, безопасностью и переносимостью, что, однако, не снижает его общую эффективность. (Степень рекомендаций 1.)
Вальпроаты
Вальпроатами (дивальпроат, дивалпроекс, вальпромид) называют различные формы 2-пропилпентаноата натрия или вальпроата натрия. Активным веществом, проникающим через гематоэнцефалический барьер, является вальпроевая кислота (вальпроат).
Различные формы вальпроатов могут отличаться превращениями в желудочно-кишечном тракте, но не влиянием на активность ЦНС (Grunze, Walden, 2004).
Вальпроат считается средством, широко применяющимся в профилактическом лечении БАР, которое было разработано как альтернатива литию. Научные данные свидетельствуют о его долговременной пользе, но не во всех странах вальпроат лицензирован для профилактической терапии БАР.
Следует отметить, что вальпроат стал широко использоваться не в связи с доказанной пользой, а благодаря испытаниям, в которых применяли дизайн прекращения наблюдений (как и для большинства первых исследований атипичных АП). Таким образом, выводы об эффективности вальпроата не являются негативными, скорее, они не окончательные (Bowden et al., 2000; Gyulai et al., 2003).
Было выявлено одно исследование, в котором изучали эффективность и переносимость продолжительного профилактического лечения вальпроатом продолжительностью 8 месяцев у пациентов с БАР I и II после перенесенного последнего депрессивного эпизода.
Сила эффекта была недостаточной, однако показана польза дополнения вальпроатом профилактической терапии ламотриджином, которая выражалась в увеличении времени до проявления любых новых аффективных эпизодов по сравнению с плацебо (Bowden et al., 2012).
Литий или вальпроат использовали в двух сравнительных испытаниях эффективности поддерживающего лечения БАР арипипразолом или зипразидоном. В исследовании арипипразола пациенты, удовлетворявшие критериям стабилизации состояния, были распределены для приема арипипразола по 10-30 мг/сут в качестве дополнения к вальпроату, литию или плацебо на протяжении 52 недель.
Дополнение арипипразола к литию имело более предпочтительные результаты относительно времени до рецидива любого аффективного эпизода по сравнению с приемом только лития, тогда как между группами арипипразол + вальпроат и вальпроат + плацебо различия отсутствовали (Marcus et al., 2011).
Схожие данные были получены в исследовании дополнения зипразидоном профилактического лечения вальпроатом или литием (Bowden et al., 2010). Испытания, в которых бы отдельно изучали эффективность профилактики депрессивных или маниакальных эпизодов, отсутствуют.
В большинстве исследований способность вальпроата предотвращать аффективные эпизоды сравнивалась с литием и плацебо (Bowden et al. 2000).
Вальпроат не отличался от плацебо по показателям профилактики любых аффективных эпизодов, однако демонстрировал превосходство по таким вторичным методикам оценки результатов, как прекращение испытаний по причине депрессии или побочных эффектов. (Уровень доказательности С при применении вальпроата для профилактики любых аффективных эпизодов, уровень доказательности В – депрессивных и уровень доказательности F – маниакальных.)
У пациентов с быстрой цикличностью вальпроат самостоятельно или в комбинации с литием не был эффективным для профилактики новых аффективных эпизодов (уровень доказательности F).
Двойное слепое сравнительное РКИ было посвящено профилактическому лечению оланзапином и вальпроатом на протяжении 47 недель у пациентов, перенесших маниакальный эпизод.
Так, при приеме оланзапина имело место более значительное снижение оценки по шкале YMRS, хотя различий в уровне последующих рецидивов не выявлено (Tohen et al., 2003).
Эффективность вальпроата в профилактике маний и депрессий отмечалась в открытых испытаниях (Lambert, 1984; Puzynski, Klosiewicz, 1984; Vencovsky et al., 1984; Hayes, 1989; Emrich, Wolf, 1992; Denicoff et al., 1997; Hirschfeld et al., 1999; Solomon et al., 1998). Однако в открытых сравнительных исследованиях вальпроат уступал литию (Kessing et al., 2011). (Оценка «+» для дополнительных доказательств.)
Обычно вальпроат хорошо переносится. Многие побочные эффекты препарата, в том числе желудочнокишечные, неврологические (тремор и легкая седация), тромбопения или лейкопения и бессимптомтомное увеличение трансаминаз печени, зависят от дозы и ослабляются при ее снижении. Тромбоцитопения и лейкопения зачастую легкие и носят обратимый характер. Может наблюдаться выпадение волос и изменение их текстуры.
Тяжелой и потенциально опасной является идиосинкратическая печеночная недостаточность, которая встречается очень редко (приблизительно один случай на 50 тыс. пациентов).
Нежелательные реакции чаще возникают у пациентов в возрасте до двух лет, при одновременном использовании вальпроата с другими противоэпилептическими средствами, а также при тяжелых заболеваниях печени или наследственных нарушениях обмена карнитина или мочевины.
Было описано несколько случаев острого геморрагического панкреатита в первые три месяца лечения (Grunze, Walden, 2004).
Вероятно, наиболее распространенным побочным эффектом длительного приема вальпроата является повышение веса, которое сравнимо с оланзапином (Tohen et al., 2003). Вальпроат нельзя применять во время беременности, а также не следует рутинным образом длительно назначать женщинам детородного возраста (Nguyen et al., 2009; Meador et al., 2009).
Вероятность взаимодействия вальпроата с другими препаратами, используемыми в лечении БАР, очень низкая. Вальпроат может усиливать седативное действие других психотропных средств. Кроме того, он замедляет метаболизм ламотриджина. Особый мониторинг необходим при комбинации вальпроата с карбамазепином. (Оценка 0 для безопасности и переносимости.)
Gibbons et al. (2009) показали, что прием вальпроата не ассоциируется с усилением суицидальных намерений, но, с другой стороны, антисуицидальное действие вальпроата значительно уступает таковому лития (Goodwin et al., 2003) (оценка 0 для профилактики суицидов).
Вальпроат доступен в виде таблеток с быстрым или длительным высвобождением, раствора для перорального приема и инъекций. Установлена зависимость между концентрацией препарата в плазме и его антиманиакальным эффектом (Allen et al., 2006).
По данным Keck et al. (2005), при применении с профилактической целью концентрация вальпроата в сыворотке крови ниже, чем при лечении больных эпилепсией – 45-100 мг/л (315-700 мкмоль/л). (Оценка «+» для практичности.)
Таким образом, незначительные доказательства использования вальпроата в профилактическом лечении БАР обусловили степень рекомендаций 3.
Антипсихотики первого поколения
Использование типичных АП (АП первого поколения) в профилактическом лечении БАР всегда вызывало трудности в связи с высоким риском экстрапирамидных побочных эффектов, следствием чего могло быть несоблюдение их приема.
Недавно появились сообщения,что длительное применение данных препаратов у больных шизофренией приводит к нейротоксическим эффектам и уменьшению объема серого вещества мозга (Lieberman et al., 2005; Ho et al., 2011; Vernon et al., 2012).
Таким образом, типичные АП также могут вызывать когнитивные нарушения, помимо тех, что наблюдаются при этом расстройстве.
Было выявлено лишь одно исследование с достаточным количеством участников, в котором изучали дополнительный прием перфеназина в лечении литием, карбамазепином или вальпроатом (Zarate, Tohen, 2004).
После достижения ремиссии маниакального эпизода 37 больных распределили для двойного слепого применения лития, карбамазепина или вальпроата с дополнением перфеназина или плацебо на протяжении 6 месяцев.
Пациенты, получавшие плацебо, с большей вероятностью завершали исследование, у них отмечалась большая продолжительность времени до рецидива депрессивного эпизода, а также они реже испытывали акинезию, дисфорию и паркинсонизм. Между группами отсутствовали различия в частоте маниакальных рецидивов. (Уровень доказательности Е для профилактики любых аффективных эпизодов.)
Не выявлены испытания, в которых бы изучали профилактическое лечение типичными АП у пациентов с быстрой цикличностью (уровень доказательности F).
В открытом исследовании при сравнении флупентиксола и лития не отмечено различий во влиянии обоих препаратов на течение заболевания (Ahlfors et al., 1981). В испытании флупентиксола деканоата (n = 93) выявили снижение частоты маниакальных эпизодов и увеличение продолжительности времени до маниакального эпизода, однако при этом значимо возрастала частота депрессивных эпизодов и сокращалось время до их возникновения.
Таким образом, флупентиксол обладает некоторым протективным антиманиакальным действием, хотя в двойном слепом сравнительном исследовании флупентиксола и лития в течение двух лет этот эффект не нашел подтверждения (Esparon et al., 1986). В ряде публикаций сообщалось, что флупентиксол может вызывать манию (Szabo, 1993; Becker et al., 2002). (Оценка 0 для дополнительных доказательств.)
Подобно АД, антиконвульсантам и атипичным АП, типичные АП не являются однородной группой препаратов. Профиль их переносимости и безопасности может отличаться.
Частота и тяжесть многих побочных эффектов лекарственных средств этой группы зависят от дозы и продолжительности приема. Ранее их часто излишне применяли для лечения острой мании.
Принято различать побочные действия типичных АП, связанные с кратковременным и долговременным лечением. Большинство типичных АП не вызывают увеличения массы тела.
По сравнению с атипичными АП прием этих препаратов связан с высоким риском злокачественного нейролептического синдрома (Tural, Onder, 2010). Препараты данной группы обладают различным риском развития серьезных врожденных аномалий при использовании во время беременности. Сравнительно безопасным считается галоперидол (Diav-Citrin et al., 2005).
Перфеназин формально не разрешен FDA для применения во время беременности. (Оценка «–» для безопасности и переносимости.)
Не было выявлено соответствующих исследований влияния типичных АП на суицидальные намерения. Есть лишь сообщение о том, что прием этих препаратов у лиц с БАР может предупреждать суициды (Angst et al., 2005). (Оценка 0 для профилактики суицидов.)
Типичные АП доступны в различных формах, в том числе в виде таблеток, растворов и инъекций короткого и длительного действия. Чаще других используется нейролептик галоперидол. Перед назначением типичных АП рекомендуется тщательное соматическое обследование для выявления сопутствующих заболеваний. В 2007 г. FDA было рекомендовано обязательно проводить ЭКГ-мониторинг у всех пациентов, принимающих галоперидол парентерально. (Оценка «+» для практичности.)
Учитывая отсутствие надежных доказательств и неблагоприятный профиль побочных эффектов, продолжительное использование типичных АП у пациентов, страдающих БАР, не может быть рекомендовано. (Степень рекомендаций ?.)
Другие атипичные антипсихотики в профилактическом лечении БАР
Амисульприд часто используется в лечении БАР. Опубликовано лишь одно открытое испытание его применения в качестве дополнения (Carta et al., 2006).
Авторы выявили значимое уменьшение общего количества рецидивов и обострения симптомов, требовавшего госпитализации, на протяжении около одного года катамнестического наблюдения. В группе плацебо риск рецидива был в три раза выше, однако значимые отличия отмечались только для маниакальных эпизодов.
При длительном приеме вполне приемлемым представляется профиль побочных эффектов препарата, однако его использование ограничено из-за риска повышения пролактина и возникновения экстрапирамидных симптомов (Rummel-Kluge et al., 2010). (Оценка «–» для безопасности и переносимости.)
В двух РКИ было доказано антиманиакальное действие при монотерапии азенапином, а также в одном исследовании с применением комбинированного лечения (Grunze et al., 2009; Szegedi et al., 2012). Согласно данным вторичных методик оценки результатов, поддерживающее лечение азенапином на протяжении одного года не уступало в эффективности оланзапину.
Однако этот вывод не является окончательным из-за значительного уровня прекращения испытаний.
Кроме того, отсутствуют результаты других исследований, которые бы подтверждали эффективность поддерживающего лечения для профилактики маниакальных эпизодов.
Из побочных эффектов длительного приема азенапина указывались повышение веса и легкая сонливость. Препарат доступен только в виде таблеток для сублингвального приема, что может быть непрактичным у некоторых пациентов.
Недавно в одном РКИ было продемонстрировано антиманиакальное действие карипразина, однако отсутствуют данные о результатах длительного приема препарата (Yildiz et al., 2011).
Несмотря на широкое использование при рефрактерном БАР клозапина, отсутствуют контролируемые плацебо испытания его применения. Фармакоэпидемиологическое исследование, проведенное в Дании, было посвящено эффективности клозапина у 326 лиц с БАР (Nielsen et al., 2012).
Во время приема клозапина у пациентов сокращались среднее количество дней госпитализации, среднее число госпитализаций и определенная дневная доза психотропных медикаментов.
Также есть несколько сообщений о серии случаев лечения клозапином больных БАР (Puri et al., 1995; Zarate et al., 1995; Hummel et al., 2002). Сообщения о сериях случаев поддерживают использование клозапина у пациентов с быстрой цикличностью (Calabrese et al., 1991; Suppes et al., 1994; Frye et al., 1996; Lancon, Llorca, 1996).
У лиц, страдающих шизофренией, было показано антисуицидальное действие клозапина, которое, однако, не изучалось при БАР.
Отсутствуют опубликованные данные исследований, поддерживающие продолжительное использование зотепина в лечении БАР, доказательства ограничиваются только лечением острой мании (Grunze et al., 2009). При длительном приеме зотепина могут наблюдаться умеренное увеличение массы тела, гиперлипидемия и седация, но в меньшей степени, чем при использовании оланзапина. Есть мало доступных данных относительно сравнения зотепина с другими атипичными АП (Riedel et al., 2010; Rummel-Kluge et al., 2010).
Другие антиконвульсанты, используемые в лечении БАР
Иногда в качестве альтернативы карбамазепину используется окскарбазепин. Возможно, что у окскарбазепина выше риск гипонатриемии (Van Amelsvoort et al., 1994). Существуют данные, поддерживающие применение этого препарата при острой мании (Grunze, 2010). Vieta et al. (2008) оценивали эффективность и переносимость окскарбазепина в профилактическом лечении БАР I и II в качестве дополнения к литию в условиях двойного слепого РКИ на протяжении одного года.
Окскарбазепин не отличался от плацебо по времени возврата симптомов любого аффективного эпизода и количеству рецидивов. Отмечалась незначимая тенденция меньшего количества депрессивных эпизодов за время катамнестического наблюдения в группе окскарбазепина. (Степень рекомендаций 4.)
Фенитоин продемонстрировал превентивное действие в небольшой выборке пациентов (Mishory et al., 2003). Так, 23 стабильных биполярных пациента, которые перенесли, как минимум, один аффективный эпизод за последние 2 года (преимущественно маниакальный), принимали на протяжении последующих 13 месяцев фенитоин или плацебо.
Фенитоин был добавлен к стандартному лечению, средняя доза препарата составила 380 ± 80 мг. В группе фенитоина в три раза реже отмечались рецидивы, причем рецидивы мании были в два раза чаще, чем таковые депрессии. (Уровень доказательности C, степень рекомендаций 4.)
Габапентин и топирамат изучались в РКИ для лечения острой мании, однако полученные результаты были неудачными (Grunze et al., 2009). Поэтому проведение дальнейших исследований не финансировалось, и поддерживающее лечение не изучалось.
Существуют данные, указывающие на некоторую эффективность топирамата, в том числе у пациентов с быстрой цикличностью, но они не позволяют сделать окончательные выводы (Marcotte, 1998). Кроме того, изучалось использование топирамата в сочетании с оланзапином для предупреждения повышения веса (Vieta et al., 2004).
Топирамат представляется практичным в использовании, для лечения БАР применяются низкие дозы препарата, однако есть опасения по поводу преходящих неврологических побочных эффектов, которые не зависят от дозы (Jones, 1998). (Степень рекомендаций 4.)
В настоящее время габапентин, как и топирамат, у пациентов с БАР используется для профилактики увеличения массы тела, а также для терапии сопутствующих тревожных расстройств и нарушений, вызванных злоупотреблением психоактивными веществами, хотя данные контролируемых исследований не поддерживают такую практику (Perugi et al., 2002; Carta et al., 2003).
Наилучшие доказательства применения габапентина в качестве дополнения при профилактическом лечении БАР были получены в небольшом двойном слепом РКИ продолжительностью 12 месяцев (Vieta et al., 2006).
К окончанию исследования в группе габапентина по сравнению с плацебо отмечались лучшие показатели по шкале общего клинического впечатления, также препарат хорошо переносился. У габапентина короткий период полувыведения, поэтому его следует принимать три раза в день. (Степень рекомендаций 4.)
Рабочей группе не удалось выявить исследований длительного использования при БАР следующих антиконвульсантов: эсликарбазепина, прегабалина, леветирацетама, вигабатрина, барбитуратов или бромидов, по крайней мере, опубликованных в период, которым ограничивался поиск литературы.
Гормоны, витамины, аминокислоты и жирные кислоты
В контролируемом плацебо исследовании изучалось дополнительное лечение N-ацетилцистеином (N-АЦ, 1 г дважды в день) у лиц с БАР (n = 75), страдавших резистентной подпороговой депрессией. После 24 недель лечения прием N-АЦ ассоциировался с улучшением оценок по шкале Монтгомери – Асберг к 20-й и 24-й неделям – у пациентов группы лечения чаще отмечался терапевтический ответ.
Однако N-АЦ не влиял на время до проявления рецидива (Magalhaes et al., 2011).
Противоречивы доказательства использования при БАР полиненасыщенных жирных кислот омега-3. Положительные результаты были получены в острой фазе терапии депрессии (Frangou et al., 2006; Keck et al., 2006). Stoll et al. (1999) указывали, что в их двойном слепом РКИ продолжительностью 4 месяца у пациентов с неполной ремиссией отмечалось значимое уменьшение периода достижения ремиссии у принимавших жирные кислоты омега-3 (9,6 г в день, что соответствует 6,2 г эйкозапентойной кислоты), которые добавлялись к стандартному лечению.
Обычно жирные кислоты омега-3 хорошо переносятся, также их прием снижает риск смерти вследствие сердечно-сосудистых заболеваний у больных аффективными расстройствами (Severus et al., 2001). (Степень рекомендаций 4.)
Поддерживающая электроконвульсивная терапия
В литературе используется несколько взаимозаменяемых терминов, обозначающих поддерживающую ЭКТ – «продолжительная» и «профилактическая» ЭКТ. Также представляется парадоксальным назначение ЭКТ у изначально стабильных эутимических пациентов.
Природа ЭКТ не позволяет проводить контролируемые плацебо исследования, поэтому для доказательств при применении этого метода отсутствует уровень доказательности A и B.
Однако существует множество открытых испытаний. Несмотря на небольшой объем выборок, в каждом из них указывалась польза использования ЭКТ в профилактическом лечении БАР после хорошего терапевтического ответа на ЭКТ в острой фазе лечения (Loo et al., 2011).
С 1998 по 2009 гг. в англоязычной литературе было выявлено 32 сообщения о применении поддерживающей ЭКТ, в которых содержалась информация о результатах терапии у 284 пациентов. В большинстве из них отмечались преимущества этого метода, однако имелись различия в протоколах применения ЭКТ (характер стимулов, частота), поэтому их сравнение не представляется возможным (Petrides et al., 2011).
В открытом исследовании у 14 пациентов с быстрой цикличностью БАР I и II без терапевтического ответа на фармакологическое лечение сеанс поддерживающей ЭКТ назначали один раз в месяц на протяжении 2 лет.
Средняя продолжительность терапии составила 21 месяц, за это время состояние всех пациентов улучшилось – уменьшилось количество дней нетрудоспособности и увеличилась продолжительность периодов без симптомов заболевания (Minnai et al., 2011).
Наибольшее беспокойство вызывают прогрессирующие когнитивные нарушения, связанные с проведением сеансов ЭКТ. Также риски этого метода могут ассоциироваться с использованием кратковременной анестезии. В сообщениях об ЭКТ эти опасения не поддерживаются, а во многих из них не применялись методики для оценки нарушений памяти. Принимая решение об использовании поддерживающей ЭКТ, клиницистам следует учитывать указанные опасения.
По сравнению с медикаментозным лечением ЭКТ требует привлечения дополнительных усилий, однако зачастую поддерживающая ЭКТ используется в амбулаторных условиях и не требует госпитализации, а частота сеансов составляет от двух в неделю до одного в месяц. (Степень рекомендаций 4.)
Другие виды биологической терапии
В острой фазе лечения депрессии часто используются депривация сна и светотерапия, однако опубликованные данные о профилактическом применении этих методов отсутствуют.
Выполнено несколько первых исследований использования в лечении БАР повторяющейся транскраниальной магнитной стимуляции, стимуляции блуждающего нерва и глубокой стимуляции мозга, но эффективность этих методов в поддерживающей терапии БАР практически неизвестна (Agarkar et al., 2011; Rush et al., 2005; Nierenberg et al., 2008).
Описано положительное влияние глубокой стимуляции мозга на симптомы депрессии у пациентов с болезнью Паркинсона, а также при рекуррентном депрессивном расстройстве (Raucher-Chene et al., 2008; Holtzheimer et al., 2012). Таким образом, доказательства использования в профилактическом лечении БАР этих методов биологической терапии представляются слабыми и недостаточными для того, чтобы рекомендовать их.
Роль психотерапии и образовательных мероприятий
Как было указано во введении, при разработке данного руководства не изучались доказательства психотерапии в продолжительном лечении БАР. Психотерапия и образовательные мероприятия играют важную роль в соблюдении приема медикаментозного лечения и повышении устойчивости пациентов к аффективным раздражителям, что задокументировано в исследованиях и интегрировано в терапии (Scott et al., 2007, 2009; Beynon et al., 2008).
Выводы
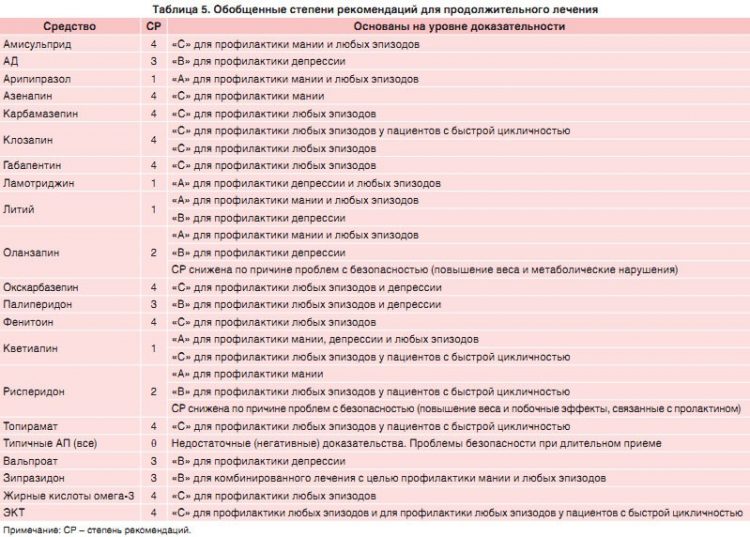
Благодаря подходу, применявшемуся при разработке серии руководств WFSBP по терапии БАР, было определено шесть медикаментов, которые рекомендованы для поддерживающего лечения БАР, два из них обладают наивысшей степенью рекомендаций.
Хотя ни одно из этих лекарственных средств не охватывает в одинаковой мере все аспекты лечения у всех групп пациентов, страдающих БАР, по сравнению с первой редакцией руководства выявлено несколько альтернатив (Grunze et al., 2004). Однако, несмотря на появившиеся альтернативы, литий сохраняет за собой место наилучшего стандарта профилактического лечения БАР.
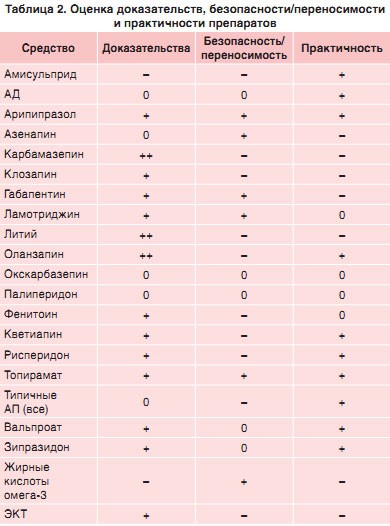
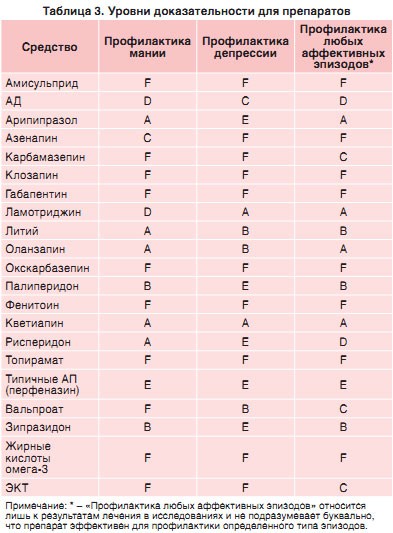
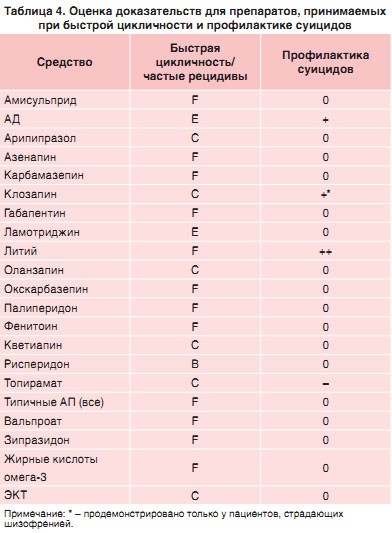
Большинство рассмотренных РКИ профилактического лечения БАР были проведены в последние два десятилетия, однако это не подразумевает, что в повседневной практике следует игнорировать «старые» средства, например карбамазепин или клозапин, по причине их меньшей эффективности или худших переносимости и безопасности. Сводные данные руководства приведены в таблицах 2-5.
Источник: https://neuronews.com.ua/